خلاصه
فناوری های پرینت سه بعدی که برای کاربردهای پزشکی استفاده می شوند، بیشتر بر پایه اکسترودرهای خمیری هستند. اینها برای ظرفیت بالا طراحی شده اند و بنابراین اغلب دارای مخازن مواد بزرگ و نازل های با قطر بزرگ هستند. یک چالش عمده برای اکثر پلتفرم های چاپ سه بعدی، مصالحه بین سرعت، دقت و/یا حجم/جرم عناصر متحرک است. برای رسیدگی به این مسائل، ما یک پمپ پریستالتیک را در یک چاپگر زیستی ادغام کردیم. این امکان ترکیب مهمترین الزامات را فراهم کرد: دقت بالا، یک مخزن بزرگ مواد و ایمنی مواد بیولوژیکی. سیستم یک نازل کاملا گرم شده و یک بستر چاپ خنک شده برای حفظ دمای هیدروژل بهینه و سرعت اتصال عرضی توسعه داده شد. اصلاحات ما در طراحی چاپگر زیستی، خواص مکانیکی پرینتها و دقت آنها را بهبود بخشید و در عین حال حداکثر میزان بقای سلولها را حفظ کرد و ظرفیت مخزن بیووئینک را افزایش داد.
کلید واژه ها:
چاپ زیستی سه بعدی ؛ اکستروژن ؛ آلژینات سدیم/ژلاتین ؛ مدل سازی و آزمایش بیواینک ; مهندسی بافت ; طراحی چاپگر زیستی
چکیده گرافیکی
1. معرفی
امروزه بسیاری از افراد در انتظار پیوند هستند و در بسیاری از موارد این تنها روشی است که می تواند جان خود را نجات دهد، مخصوصاً در مورد مهم ترین اعضای بدن مانند قلب، کلیه یا کبد. متأسفانه، اندام های اهداکننده کافی برای رفع نیاز موجود نیست. ساختارهای بافتی لوله مانند ساده در حال حاضر قابل چاپ هستند، اما اندام های کاملاً کاربردی هنوز قابل چاپ نیستند. با این حال، توسعه چاپ زیستی سال به سال این امید را بیشتر و بیشتر می کند که تولید اعضای بدن برای بیماران فردی امکان پذیر باشد. چاپ زیستی یکی از شاخه های بیولوژیکی پرینت سه بعدی است. در این تکنیک، لایههای یک ماده یکی بر روی دیگری قرار میگیرند تا اجسام سهبعدی را یکی یکی بسازند. ماشینهای چاپ زیستی مستقیم از مواد زیستی قابل چاپ با رنگ زیستی مخلوط با سلولهای زنده یا ترکیبات فعال بیولوژیکی استفاده میکنند. متداول ترین بیومواد مورد استفاده هیدروژل ها هستند، مانند آلژینات سدیم و/یا ژلاتین. چنین مخلوط هایی به منظور ارائه سرعت بالای تولید مثل سلول و قابلیت چاپ خوب هستند. جدا از سازگاری زیستی، ویسکوزیته هیدروژل نیز یک جنبه مهم است، زیرا نه تنها بر فرآیند چاپ (قابلیت چاپ) بلکه بر تکثیر سلولی نیز تأثیر می گذارد [ 1 ، 2 ].
چندین تکنیک چاپ وجود دارد. پرطرفدارترین روش چاپ زیستی مبتنی بر اکستروژن (EBB) است که در آن بیووینک از طریق نازل متصل به سر چاپ رانده می شود. قطر نازل ها به ندرت بیشتر از 400 میکرومتر است. این برای ایجاد کرنش ماده به اندازه کافی نازک برای ساخت هندسه های پیچیده و به اندازه کافی ضخیم است که به سلول های معلق در بیوینک توسط فشار اکستروژن بسیار زیاد و/یا قطر مویرگی خیلی کوچک آسیب نرساند [ 3 ، 4 ، 5 ]. علاوه بر این، این روش تغذیه مواد در معرض طیف وسیعی از محدودیتهای عملکردی است، اغلب با سرعت پایین چاپ میشود و فقط هندسههای ساده ایجاد میکند. اکثر اکسترودرهای مبتنی بر سیال عملکرد عقب نشینی که حرکت معکوس مواد (اکستروژن معکوس) است را ندارند. حرکات غیر اکسترود ممکن است منجر به نشت یا تراوش ناخواسته شود که می توان با جمع کردن مواد از آن جلوگیری کرد، بنابراین از نتایج بد چاپ مانند کیفیت پایین، برآمدگی گوشه ها، اکستروژن بیش از حد، و عیوب مانند رشته های نازک و از نوع سبیل جلوگیری کرد. . ایده هایی در مورد راه های ممکن برای مقابله با این مشکل وجود دارد. به عنوان مثال، سیستم Envision TEC Bioplotter [ 6 ] دارای انبار تمیز کردن خودکار نازل است که بین لایههای بعدی در طول چاپ استفاده میشود. به لطف این راه حل، کیفیت چاپ افزایش می یابد، با این حال، زمان چاپ حتی چاپ های کوچک به طور قابل توجهی افزایش می یابد. در مورد چاپ با بیواینک (پرینت زیستی مستقیم) چنین اثری نامطلوب است. با در نظر گرفتن این نوع ناراحتی، ما سیستم پرینت سه بعدی خود را عقب نشینی کردیم و بنابراین می تواند اشیاء پیچیده را بدون ترشح قابل توجهی از مواد چاپی چاپ کند. از آنجایی که پمپ پریستالتیک موادی را از مخزن تحویل میدهد که میتوان آن را در حین چاپ دوباره پر کرد، سیستم پتانسیل چاپ اشیاء با حجم بالا را دارد.
اکسترودرهای پمپ سرنگی که در حال حاضر مورد استفاده قرار میگیرند، عمدتاً دارای وضوح بالا یا حجم کم هستند که به دلیل سازش بین جرم متحرک و دقت موقعیتیابی بالا است. بنابراین، سیستم های چاپ زیستی تجاری معمولاً مخازن مواد 10 میلی لیتری را برای کاهش جرم کالسکه اجرا می کنند. با این حال، این راه حل اندازه چاپ را محدود می کند.
اکسترودر معرفی شده توسط Hinton و همکاران، همراه با سیستم چاپ سه بعدی FRESH به نام Replistruder، دقیقاً سازش بین دقت و جرم متحرک چاپگرهای زیستی را نشان می دهد [ 7 ]. Replistruder برای ارائه قابلیت جمع کردن مواد زیستی طراحی شده است، اما توانایی آن برای چاپ اجسام بزرگ به دلیل استفاده از حداکثر 10 میلی لیتر مخزن مواد چاپی محدود است. اصلاحات Replistuder با هدف افزایش حجم سرنگ انجام شده است، با این حال، وزن اضافی اضافی که به کالسکه وارد می شود ممکن است بر عملکرد چاپ تأثیر منفی بگذارد. کامپتون و لوئیس یک اکسترودر سرنگ با دقت بالا را توسعه دادند که توسط پنوماتیک هدایت می شود [ 8 ]. امکان چاپ با استفاده از پلیمر یا اپوکسی با کیفیت بالا با استفاده از مخزن مواد کم حجم را داشت، اما به دلیل مواد استفاده شده نمی توان آن را چاپگر زیستی نامید. در حالی که اکسترودرهای خمیر تجاری، مانند Fab@Home Scientist Printer [ 9 ]، PrintrBot Paste and Extruder [ 10 ]، Discovery Paste Extruder [ 11 ] یا ZMorph Thick Paste Extruder [ 12 ]، دارای سرنگ های 30 تا 100 میلی لیتری هستند، اما سرنگ های مخزن دارند. آنچه را که در حجم به دست می آورند، در کارایی و دقت از دست می دهند. این سیستم ها معمولاً با نازل هایی با قطر زیاد کار می کنند. رزولوشن را کاهش می دهد و فرآیند چاپ را کم تقاضا می کند، اما در عین حال این ماشین ها با سرعت کم چاپ می کنند تا بارهای سنگین تر خود را جبران کنند [ 13 ، 14 ، 15 ، 16 ، 17 ]. روش اکسترودر Bowden می تواند برای کاهش جرم بیش از حد بر روی عناصر متحرک استفاده شود. این نوع سیستم مخازن مواد را از طریق یک لوله به نازل متصل می کند و از کاهش زیاد سرعت جلوگیری می کند. چنین سیستمهایی معمولاً به صورت پنوماتیک هدایت میشوند، اما دارای نقاط ضعفی هستند، از جمله فشار اکستروژن، که بسته به مقدار مواد باقیمانده در مخزن و نیاز به خلاء دقیق در حین چاپ برای امکان پسکشی متفاوت است. سیستمهای با هدایت پنوماتیک همچنین دارای تأخیرهای پاسخ نیرو هستند که هم به خواص رئولوژیکی (مثلاً نیوتنی، نازک شدن برشی، تیکسوتروپی) ماده اکسترود شده و هم به حجم مخزن مواد بستگی دارد. سیستم های هدایت پنوماتیک نیز گران و حجیم هستند، زیرا نیاز به منبع فشار هوا جداگانه دارند که هزینه کلی را افزایش می دهد، فشردگی سیستم را کاهش می دهد و کل ساختار را بدون افزایش قابلیت استفاده پیچیده می کند. در سیستم ما که از یک اکسترودر به سبک Bowden استفاده می کند، پیستون توسط یک موتور پله ای حرکت می کند که فشار اکستروژن و عقب نشینی ثابتی را فراهم می کند.
دانشمندان در سراسر جهان در حال بهبود و توسعه چاپگرهای زیستی خود هستند. توسعه سریع در زمینه چاپ زیستی و نیاز آشکار در این زمینه با تعداد کتاب ها و مقالاتی در این زمینه که اخیراً منتشر شده است نشان می دهد، به عنوان مثال، “چاپ اندام” یکی از جدیدترین ها است [ 18 ]، و همچنین بررسی های علمی مانند بررسی مورفی و آتالا [ 19 ]. همانند سایر تکنیکها و شاخههای پرینت سه بعدی، چاپ زیستی سازگاریها و تحولات خود را نیز دارد. یکی از نمونه ها روش ترکیبی چاپ زیستی است که ترکیبی از مدل سازی رسوب ذوب شده برای تولید داربست زیست تخریب پذیر جامد با چاپ زیستی زیستی همزمان است. این رویکرد توسط گروه مالدا در دانشگاه اوترخت (هلند) [ 20 ] و بعداً توسط گروه آتالا در دانشگاه ویک فارست در کارولینای شمالی (ایالات متحده آمریکا) [ 21 ] توسعه یافت. میرونوف و همکاران در سال 2003 مفهومی از تولید افزودنی سه بعدی چاپ اندام بر اساس کره های بافتی را به عنوان بلوک های سازنده برای غلبه بر تراکم سلولی کم در بیوئینک معرفی کرد [ 22 ]. Organovo Holdings Inc. (ایالات متحده آمریکا) که روش اصلی چاپ زیستی بافت را با استفاده از کروی فرموله کرد، نتوانست این فناوری را تکرارپذیر کند زیرا کرویهای بافت معمولاً قبل از توزیع با هم ترکیب میشوند. دانش ثبت شده توسط گروه Forgacs در دانشگاه میسوری (کلمبیا، ایالات متحده آمریکا) و گروه Mironov در دانشگاه پزشکی کارولینای جنوبی (چارلستون، ایالات متحده) توسعه یافته است. تیم ها بر روی چاپ ساختار لوله مانند با استفاده از تکنیک های مختلف چاپ سه بعدی کار کردند. گروه Forgacs و Organovo توزیع مداوم میله ای را توسعه دادند که امکان آماده سازی لوله عمودی را فراهم می کرد [ 23 ]. گوئرا و همکاران روی داربست های زیست سازگار پرینت سه بعدی با قطر 8 میلی متر یا کمتر کار می کنند [ 24 ]. چاپگر زیستی طراحی آنها بر اساس تکنیک مدلسازی رسوب ذوب شده (FDM) و فناوریهای چاپ سهبعدی 3 محوره ساخته شده است. ایده این است که مواد از نازل اکسترودر عبور می کنند، که مواد را روی یک محور چرخشی افقی کنترل شده توسط کامپیوتر قرار می دهد و یک بستر چاپ را تشکیل می دهد. گروه گائو از دانشگاه ژجیانگ (چین) از رویکرد مشابهی استفاده می کند [ 25]. در محلول آنها یک سیستم سوزن کواکسیال اعمال می شود، جایی که سوزن بیرونی هیدروژل را فراهم می کند، و سوزن داخلی برای ارائه یک عامل اتصال عرضی استفاده می شود. این فرآیند ساختارهای لوله مانند مانند چاپ با کانال های سیال در داخل ساختارها را ایجاد می کند. تیمهای دیگر یک رویکرد غیرداربستی برای چاپ سهبعدی مانند فناوری جدید پلت فرم بدون داربست «Kenzan» بر اساس مجموعهای از سوزنهای جراحی برای مونتاژ روباتیک کرویهای بافت ایجاد کردند. آنها از یک دستگاه رباتیک “انتخاب و مکان” مطابق مدل دیجیتالی از پیش طراحی شده استفاده می کنند که توسط Cyfuse Biomedical KK (ژاپن) معرفی و تجاری سازی شده است [ 26 ، 27 ]. رویکرد دیگری برای چاپ زیستی غیرداربستی توسط سه گروه شامل گروه Woodfield در دانشگاه Otago (نیوزیلند) [ 28 ]، گروه Zimmermann و Koltay از دانشگاه فرایبورگ (آلمان) [ 29 ] و گروه Mironov ارائه شده است. رویکرد دیگر توسط راه حل های چاپ زیستی سه بعدی (روسیه) [ 30 ] نشان داده شده است. این شرکت سعی کرده است چاپگرهای زیستی سه بعدی نوع اکستروژن را توسعه دهد که قادر به توزیع تک کروی در یک زمان با استفاده از دستگاه میکروسیال داخلی است. گروههای Woodfield و Zimmermann و Koltay قصد دارند این نوع پیشرفته از چاپگرهای زیستی سه بعدی اکستروژن را تجاری کنند، که در ترکیب با عملکردهای قبلی به دست آمده، میتواند به استاندارد جدیدی با دو عملکرد اصلی تبدیل شود: چاپ زیستی سه بعدی مواد زیستی مخلوط با سلولهای زنده و چاپ زیستی سه بعدی از اسفروئیدهای بافت. .
چندین شرکت وجود دارد که خدمات پیچیده ای را برای پرینت زیستی سه بعدی ارائه می دهند، از جمله چاپگرها، مواد چاپی و پشتیبانی فنی [ 31 ، 32 ]. هزینه چاپگرهای زیستی سه بعدی تجاری از 10000 دلار تا بیش از 200000 دلار متغیر است. این نوع ماشین ها معمولاً امکان ایجاد تغییرات در سخت افزار و نرم افزار را ندارند. همه این مسائل مانع از نوآوری ها می شود. به همین دلیل است که این زمینه تحقیقاتی عمدتاً در سطح دانشگاهی باقی می ماند و در آزمایشگاه ها برای بررسی تکنیک های جدید بدون استفاده از ماشین های تجاری استفاده می شود. هنوز هم ورودی های زیادی برای توسعه فناوری چاپ زیستی مورد نیاز است، به طوری که چاپگرهای زیستی می توانند به محصولاتی در بازار تبدیل شوند که تولید ساختارهای بافت عملکردی را امکان پذیر می کنند.
ما در کار خود دستگاه هایی را در نظر می گیریم که قبلاً پیاده سازی شده اند و به صورت تجاری در دسترس هستند یا حداقل در حال توسعه هستند. هدف اصلی تلاشهای ما طراحی سیستمی بود که در آن بتوانیم: (1) هزینه و دشواری ایجاد آن را با استفاده از تکنیکهای چاپ سه بعدی در فرآیند تولید پمپ پریستالتیک به حداقل برسانیم. (2) حجم مخزن جوهر چاپگر زیستی را افزایش دهید. (3) با استفاده از دانش اولیه خواص بیوئینک، بستری برای تغییر قابل اعتماد، سریع و آسان مشخصات چاپگر فراهم می کند. در نتیجه، ما یک سیستم پرینت زیستی سه بعدی ارزان قیمت (حدود 500 دلار برای کل سیستم) با اکسترودر پمپ پریستالتیک منبع باز یکپارچه ایجاد کردیم که می تواند جمع شود، با سرعت متوسط کار کند و اجسام پیچیده را با روش ساخت افزودنی بسازد. چاپگر زیستی دارای یک مخزن زیستی هم زده و گرم شده است که می تواند در طول فرآیند چاپ دوباره پر شود. در نتیجه، سیستم به طور بالقوه می تواند اجسام با حجم زیاد تولید کند. علاوه بر این، این سیستم قادر به ارائه دقت چاپ بالا است و می تواند با اکثر چاپگرهای سه بعدی رومیزی منبع باز استفاده شود.
2. مواد و روشها
ساخت پرینتر سه بعدی: جرم عناصر متحرک به حداکثر کاهش می یابد. دستگاه قادر به پس زدن است، ارزان است و بر اساس یک سیستم عامل منبع باز است. برای سهولت ساخت، نصب و بهره برداری توسط کاربر معمولی طراحی شده است. عناصر اساسی این سیستم به صورت سه بعدی پرینت شدند. به همین دلیل هزینه های ساخت و ساز کم است و اصلاح آن ساده است. قطعات غیر چاپی شامل سخت افزار استاندارد مانند بلبرینگ، مهره و پیچ و مهره M3 و M5 و لوله پلی اورتان با اتصال دهنده می باشد. قطعات چاپی با استفاده از فیلامنت چاپ سه بعدی ABS (شرکت Wolfix، ورشو، لهستان) تولید شدند.
برای مقاصد چاپ زیستی، اجزای زیر سیستم طراحی و بهینهسازی شدند: یک پمپ پریستالتیک ( بخش 2.1 )، یک نازل با جریان شبیهسازی شده و گرمکننده آن ( بخش 2.2 و بخش 2.3 )، یک مخزن بیواینک ( بخش 2.4 )، و یک چاپ خنکشده تخت ( بخش 2.5 ). با استفاده از هیدروژل ها ( بخش 2.6 آماده سازی مواد زیستی) و چاپ های ساخته شده از آنها، راه حل های پیشنهادی برای دقت چاپ ( بخش 2.7 )، چسبندگی لایه ( بخش 2.8 ) و تأثیر پارامترهای چاپ بر روی زنده ماندن سلول های قرار داده شده در یک هیدروژل ( بخش 2.9 ) آزمایش شدند. .
مواد اکسترود شده-هیدروژل: تمام آزمایشها با هدف کالیبراسیون و تأیید صحت و اثربخشی ساختار چاپگر سه بعدی با استفاده از هیدروژلهایی با دو ترکیب مختلف انجام شد: 5% w/v آلژینات و 3% w/v ژلاتین (با علامت 5A3G)، و 6% w/v آلژینات و 4% w/v ژلاتین (با علامت 6A4G). هر دو در آب دیونیزه (رسانایی 0.07 میکروS) حل شدند. آلژینات سدیم (Sigma-Aldrich, Saint Louis, MO, USA)، ژلاتین (Sigma-Aldrich, Saint Louis, MO, USA) و کلرید کلسیم به عنوان پیوند متقابل (Sigma-Aldrich, Saint Louis, MO, USA) استفاده شد. برای آزمایش زنده ماندن سلول های اندوتلیال، خط EA.hy926-ATCC® CRL -2922™ (استانداردهای LGC، لندن، انگلستان) استفاده شد. این مواد در مرحله دوم برای تأیید اصلاحات معرفی شده در طرح توسعه یافته مورد استفاده قرار گرفتند که شامل: پمپ پریستالتیک ( بخش 3.1 )، تجزیه و تحلیل جریان در نازل ( بخش 3.2 )، حامل نازل و بلوک گرمایش ( بخش 3.3 )، خنک شده بستر چاپ ( بخش 3.4 )، دقت چاپ ( بخش 3.5 )، چسبندگی لایه ( بخش 3.6 ) و زنده ماندن سلول ( بخش 3.7 ).
2.1. پمپ شامل
این سیستم از پنج بخش اصلی تشکیل شده است: (1) محفظه پمپ، که شیلنگ را پشتیبانی می کند ( شکل 1 C)، (2) یک روتور مجهز به غلتک هایی که توسط موتور حرکت می کنند ( شکل 1 B)، (3) یک شیلنگ. برای انتقال هیدروژل، (4) یک نازل برای اکسترود کردن مواد و (5) یک نگهدارنده نازل ( شکل 1 D). پمپ طراحی شده با قطر خارجی شیلنگ برابر با 6.4 میلی متر سازگار بود. این اندازه لوله اجازه می دهد تا میکرو اکستروژن یکنواخت مناسب از طریق سوزن هایی با قطرهای مختلف انجام شود. سیستم ساخته شده برخلاف اکسترودرهای گذشته که معمولاً از نازل هایی با قطر حداکثر 4 میلی متر استفاده می کردند، با سوزن هایی با اندازه های مختلف سازگار بود. برای تولید پرینت، از یک سوزن نوک فولادی ضد زنگ با قطر داخلی 300 تا 620 میکرومتر استفاده کردیم. بنابراین، سیستم ترکیبی ما برای ارائه اکستروژن با حجم زیاد در معرض مصالحه بین اندازه چاپ و جزئیات آن قرار نگرفت که اغلب اکسترودرهای سرنگ تجاری را محدود میکند.
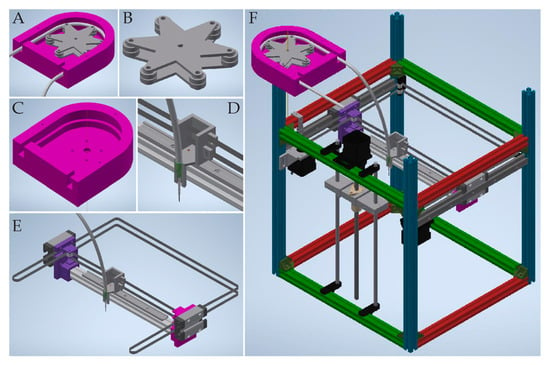
شکل 1. اجزای پمپ پرینت سه بعدی و محور X، جایی که نازل ثابت است، در نرم افزار CAD (طراحی به کمک رایانه) مدل شده است. ( A ) پمپ پریستالتیک مونتاژ شده مورد استفاده در سیستم برای اکسترود هیدروژل، ( B ) روتور مجهز به غلتک، ( C ) هسته پمپ، ( D ) نگهدارنده نازل با نازل گرم شده و اتصال تسمه تایم، ( E ) مونتاژ X- محور چاپگر، ( F ) نمای کلی طراحی چاپگر سه بعدی.
2.2. نگهدارنده نازل
این سیستم عمدتاً برای کار با چاپگرهای سه بعدی با سینماتیک هسته XY و دارای فناوری خطی طراحی شده است، زیرا نرمترین و مطمئنترین حرکت را برای انواع سیستمها ارائه میدهد. علاوه بر این، چنین چاپگرهای سه بعدی یکی از بالاترین سفتی ساختاری را داشتند. از آنجایی که قطعات متحرک سیستم به شدت کاهش یافته بودند، چاپگر می توانست با سرعت و شتاب بیشتری کار کند. بر این اساس، حامل می توانست سریع و با دقت بالا متوقف شود که منجر به بهترین حرکات چاپی ممکن و نقشه برداری مدل شد. حرکت موتورها از طریق سیستم تسمه دندانه دار GT2 به حامل منتقل می شد.
2.3. نازل کاملا گرم با جریان قابل کنترل
شیلنگ با یک قفل Luer به پایان می رسد تا امکان اتصال نازلی با قطر داخلی خاص را فراهم کند. نازل دارای تنظیم دما بود، به طوری که ویسکوزیته هیدروژل را می توان برای اطمینان از اکستروژن بهینه بیوئینک کنترل کرد. علاوه بر این، شرایط حفظ شده، محیط بهتری را برای سلول ها فراهم کرد. علاوه بر این، نازل گرم شده اجازه غلظت بالاتری از ژلاتین را می دهد که به طور مثبت تکثیر سلولی را تحریک می کند [ 33 ]. نازل در بلوک گرمایش نصب شد. این امر دمای ماده عبوری را کنترل میکرد و بنابراین اکستروژن مداوم و یکنواخت بیوئینک با دامنه وسیعی از ویسکوزیته و غلظتهای مختلف سلول امکانپذیر بود.
اکستروژن مواد با عملکرد پمپ پریستالتیک برای تامین افزایش فشار مجبور شد، که امکان تامین بیواینک را با نرخ خاصی به منطقه چاپ فراهم میکرد. علیرغم این واقعیت که نرخ جریان کم بود، فشار لازم برای غلبه بر مقاومت جریان می تواند قابل توجه باشد، به دلیل ویسکوزیته بالای هیدروژل ها و استفاده از لوله با قطر کم. عنصر کلیدی نازل به شکل یک مویرگ با قطر داخلی بسیار کوچک و طول قابل توجهی بود. با توجه به اینکه شیلنگ و سایر عناصر متصل کننده پمپ و نازل قطر بسیار بالاتری داشتند، می توان از مقاومت آنها چشم پوشی کرد.
به منظور تعیین افت فشار در نازل، ویسکوزیته دقیق هیدروژل باید شناسایی می شد. رئومتر RheolabQC (Anton Paar GmbH، Graz، اتریش) برای تعیین منحنی های ویسکوزیته در مقابل نرخ برش سیالات استفاده شد.
در این مورد، روابط ساده جریان هاگن-پوازوی برای جریان آرام سیالات نیوتنی را نمی توان اعمال کرد. بنابراین، شبیهسازی جریان هیدروژلها در نازل با نرمافزار ANSYS Workbench 19.2 (19.2 Release, Ansys Inc., Canonsburg, PA, USA) انجام شد. برای تعیین طول ورودی مویین، انتقال بین شیلنگ و نازل در نظر گرفته شد. هندسه مدل عددی و مش محاسباتی در ناحیه ورودی نازل در شکل 2 الف، ب نشان داده شده است. جریان دو بعدی در نظر گرفته شد و جریان جزء در جهت محیطی را نادیده گرفت. آزمایشهای اصلاح متوالی مش محاسباتی امکان دستیابی به راهحل مستقل مش را فراهم کرد.
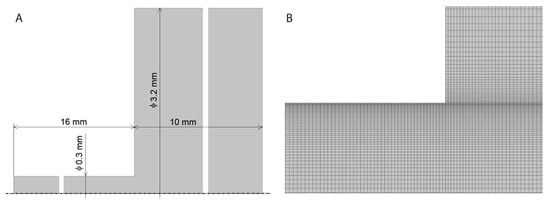
شکل 2. ( الف ) طرحی از هندسه حوزه جریان. ( ب ) مش محاسباتی در ورودی نازل.
شبیهسازی جریان حالت پایدار هیدروژلهای 5A3G و 6A4G با حلکننده ANSYS CFX 19.2 (19.2 Release, Ansys Inc., Canonsburg, PA, USA) انجام شد. به طور کلی فرآیندهای پرینت سه بعدی گذرا هستند، اما جریان های نازل از نظر زمانی در دوره های نسبتا طولانی تغییر نمی کنند، بنابراین می توان آنها را به عنوان حالت پایدار تقریب زد [ 34 ، 35 ]. هیدروژل ها تراکم ناپذیر و همدما و چگالی ثابت در نظر گرفته شدند (φ = 1600 کیلوگرم بر متر مکعب ). با در نظر گرفتن قطر نازل کوچک (D = 300 میکرومتر)، سرعت جریان کم (v ave = 2 میلیمتر بر ثانیه) و ویسکوزیته بالا، جریانها به صورت آرام با اعداد رینولدز بودند.Re = ( vخیابانD ) / μ ≤2× 10– 3Re= (vخیابانD�)/� ≤ 2×10–3. در شبیهسازیها، ویسکوزیته سیال بر اساس دادههای اندازهگیری نشاندادهشده در نمودار نشاندادهشده منحنیهای جریان (ویسکوزیته موثر در برابر نرخ برش) برای هر دو هیدروژل در بخش 3.2 تعریف شد .
شرایط مرزی برای سرعت جریان جرمی که با سرعت متوسط در نازل V ave = 2 میلیمتر بر ثانیه مطابقت دارد، بر ورودی اعمال شد. فشار مطلق (100 کیلو پاسکال) به خروجی اعمال شد. شرایط عدم لغزش روی دیوارها تنظیم شده بود.
2.4. مخزن بیواینک
مخزن زیستی محدود یکی از بزرگترین مشکلات سیستم های در حال استفاده است. سیستم ما به طور خاص برای حل این مشکل طراحی شده است. بخش اصلی سیستم یک پمپ پریستالتیک بود که امکان اکستروژن و همچنین عقب نشینی را فراهم می کرد. پمپ پریستالتیک و مخزن بیواینک در یک محفظه ایزوله حرارتی قرار گرفتند. دمای داخل آن توسط صفحه گرمایش با ترمیستور تنظیم می شد. مخزن به طور مداوم و به آرامی در محیط کنترل شده به هم زده می شد، دمای خاص را حفظ می کرد و می توانست به راحتی در طول فرآیند چاپ دوباره پر شود. موارد فوق از مواد در برابر لایه برداری محافظت می کند و از افتادن سلول ها به ته مخزن و ایجاد گلوله ها (که منجر به توزیع غیریکنواخت سلول ها در چاپ می شود) جلوگیری می کند. سیستم ما تضمین کرد که مواد بیولوژیکی به طور یکنواخت در کل حجم بیوئینک در طول کل فرآیند چاپ توزیع شده است. مخلوط جمع آوری شد، با عملیات پمپ منتقل شد و از طریق لوله و نازل روی تخت چاپ قرار گرفت. کل سیستم شرایط دمایی پایداری را برای مخزن، شلنگ و نوک نازل فراهم کرد تا از پارامترهای کافی برای بقای سلول و خواص هیدروژل اطمینان حاصل شود.
2.5. تخت چاپ سرد
چاپگر زیستی سه بعدی مجهز به بستر چاپی خنکشده مبتنی بر سلول پلتیر 60 واتی بود. اندازه سلول 40 × 40 میلی متر با یک صفحه مسی 2 میلی متری در بالای آن بود. دارای مسیری برای ترمیستور حفر شده در وسط و شیشه 2 میلی متری در بالای تخت چاپ برای بهبود چسبندگی بین هیدروژل و سطح بستر چاپی بود. همه لایه ها با خمیر رسانای گرما با رسانایی حرارتی 4.2 W/mK به هم متصل شدند. ابعاد تخت چاپ به دلیل تغییر لایه، 35 × 40 میلی متر بود. این سیستم اجازه انجماد فوری ژلاتین در هیدروژل را بلافاصله پس از چاپ می داد.
2.6. تهیه بیواینک
Bioink برای بررسی کارایی ساختار چاپ سه بعدی از نظر امکان اکستروژن ایمن مواد هیدروژل حاوی سلولهای زنده مورد استفاده قرار گرفت. طبق روشی که در مقاله قبلی ما توضیح داده شد، که در آن تست زنده بودن [ 33 ] انجام شد، تهیه شد. به طور خلاصه: آلژینات سدیم، ژلاتین و کلرید کلسیم با نور UV C به مدت 60 دقیقه استریل شدند. سپس 5% وزن/حجم آلژینات سدیم و 4% وزنی/حجم ژلاتین در محیط Eagle تغییریافته Dulbecco (DMEM, Corning Incorporated, Corning, NY, USA) همراه با 10% سرم جنین گاو (FBS) هم زده شدند (Corning Incorporated, Corning, NY، ایالات متحده آمریکا) و 1٪ آنتی بیوتیک پنی سیلین/استرپتومایسین (P/S) (Corning Incorporated، Corning، NY، USA)، گرم کردن کل سیستم تا 37 درجه سانتیگراد. سلولهای اندوتلیال، خط EA.hy926-ATCC® CRL -2922™ (استانداردهای LGC، لندن، انگلستان) همجوار در سطح 80 درصد تحت تریسینیزاسیون قرار گرفتند و سپس در محیط کشت کامل به حالت تعلیق درآمدند. سلول های آماده شده به مدت 5 دقیقه در 180 گرم سانتریفیوژ شدند. مایع رویی جمع آوری شد و محلول هیدروژل به گلوله سلولی باقی مانده در لوله شاهین وارد شد. مخلوط به صورت دستی پیپت شد تا مخلوط شود. بیووینک از طریق سانتریفیوژ کردن گاز زدایی شد تا اکستروژن یکنواخت و بدون وقفه در جریان مواد ایجاد شود.
2.7. تأیید صحت چاپ
اثرات یک بستر چاپ سرد و دمای نازل بر روی اکسترودپذیری هیدروژل 5A3G و 6A4G و دقت چاپ بررسی شد. هندسه های مختلف با چاپ تک خطی و شبکه چند لایه چاپ شدند. ارتفاع شبکه تا 11 میلیمتر بود که با 57 لایه مطابقت دارد و به ارتفاع یک لایه جداگانه و قطر نازل بستگی داشت که میتوان آن را به نیازهای کاربر تغییر داد. اولین لایه مدل با سرعت 3.5 میلی متر بر ثانیه و لایه های بعدی با سرعت 5 میلی متر بر ثانیه چاپ شد. سرعت پایین چاپ لایه اولیه از شیوه های خوب در تولید افزودنی پیروی می کند. این اجازه می دهد تا چسبندگی بهتر چاپ به تخت را به دست آورید اما هیچ یک از ویژگی های چاپ را تحت تأثیر قرار نمی دهد. این پارامترهای ساخت برای هر یک از چاپ های تولید شده ما استفاده شد.
تابع پسرفت برای هر لایه استفاده شد. به طور خودکار در محل تلاقی خطوط محاسبه شد ( شکل 3 ج) و به شرح زیر انجام شد: هنگامی که نازل حرکت چاپی انجام می دهد و به یک خط عمود می رسد، مواد جمع می شوند. نازل یک حرکت غیر چاپی انجام می دهد، یعنی به سمت محور Z حرکت می کند (بالای خط قبلاً چاپ شده حرکت می کند). سپس در محور Z به پایین می لغزد و پسرفت معکوس را انجام می دهد و حرکت چاپ را شروع می کند.
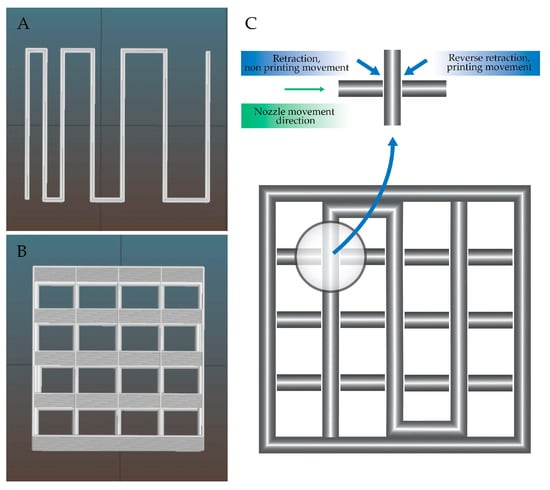
شکل 3. مدلهای آزمایش توزیع بیواینک و دقت پرینتهای فضایی: ( A ) تک خط، ( B ) شبکه چند لایه و ( C ) تجسم نحوه اعمال تابع پسکشی به مدل چاپ شده.
اجسام ساخته شده با استفاده از کولیس با وضوح 0.02 میلی متر اندازه گیری شدند. اندازه گیری ها در جهت X، Y و Z نمونه انجام شد. در مجموع پنج نمونه سه بار در هر جهت اندازه گیری شد. آزمایش ها بر روی یک چاپ تک خطی و شبکه چند لایه انجام شد. ابعاد مدل آزمایش شده عبارت بودند از: 12.5 × 12.5 × 0.35 میلی متر (XYZ) ( شکل 3 A) و 13.6 × 13.6 × 11 میلی متر (XYZ) ( شکل 3 B).
2.8. تست چسبندگی لایه
چسبندگی لایه به لایه استحکام چاپی ساختاری را تعیین می کند [ 36 ]. عناصر پرینت سه بعدی کمترین دوام را در اتصال لایه دارند، بنابراین تعیین استحکام این اتصال به ما امکان می دهد قدرت کل مدل را محاسبه کنیم. پرینت های تست چسبندگی لایه به صورت یک الگوی تک لایه چاپ شدند. خطوط پرینت یکی در کنار دیگری چاپ شده اند، به گونه ای که خط اول در تمام طول خود به خط بعدی (طول 10 میلی متر تک خط) می چسبد و صفحه مکعبی را با ابعاد 30 × 10 × 0.35 میلی متر بدون شکاف ایجاد می کند. . هندسه پرینت به گونه ای طراحی شده بود که خطوط 10 میلی متری چاپ شده بر محور بلندتر چاپ عمود باشند ( شکل 4 ). پرینتها تحت آزمایش کشش با سرعت استاتیکی 0.1 میلیمتر بر ثانیه بر روی tribotester (UMT-2، Bruker، Billerica، MA، USA) قرار گرفتند. در زمان تست استحکام کششی، مدل مانند سازدهنی کشیده شد که اجازه لایه برداری لایه بر روی تغییر لایه را می داد. آزمون ها پنج بار انجام شد و مقدار متوسط محاسبه شد. ماده مورد استفاده برای آزمایش 5A3G بود.
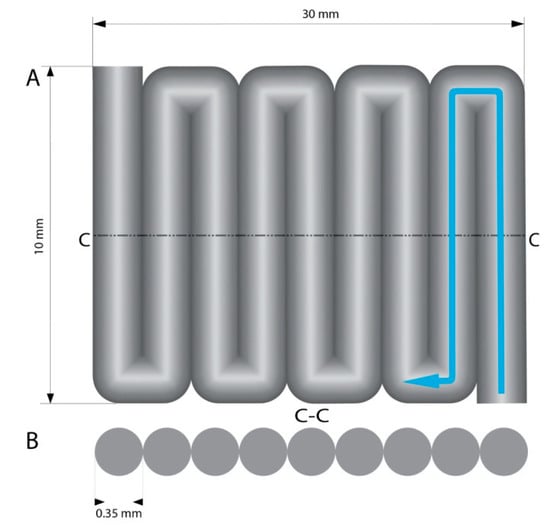
شکل 4. ( الف ) مدل برای آزمایش چسبندگی لایه. ابعاد اصلی: 30 میلی متر طول، 10 میلی متر عرض، 0.35 میلی متر ارتفاع. فلش رد شماتیک حرکت نازل را در حین چاپ نشان می دهد. ( ب ) نمای مقطع مدل ( CC ). قطر مسیر چاپ شده برابر با 0.35 میلی متر است.
2.9. تست زنده ماندن سلول ها در پرینت های ساخته شده از هیدروژل
به منظور بررسی تأثیر پارامترهای چاپ بر روی زنده ماندن سلولهای قرار داده شده در یک هیدروژل، تجزیه و تحلیل زنده/مرده برای بیوئینک پر از سلول و برای چاپها انجام شد. کل سیستم (دستگاه، سیمها، تخت چاپ و قاب دستگاه) استریل شد تا از شرایط چاپ ضد عفونیکننده اطمینان حاصل شود. پرینت های آماده شده (با یون های کلسیم به صورت متقاطع) با دو رنگ رقیق شده در بافر PBS (Corning Incorporated, Corning, NY, USA) رنگ آمیزی شدند: کلسین و همودایمر اتیدیوم (Biotium Inc., Fremont, CA, USA). محلول رنگ آمیزی 4 میلی مولار کلسین AM و 2 میلی مولار EthD-III با مخلوط کردن کامل تهیه شد. نمونه های غوطه ور در محلول رنگ آمیزی به مدت 30 دقیقه در تاریکی انکوبه شدند. چاپ های رنگ آمیزی شده با استفاده از میکروسکوپ فلورسانس (NIKON Eclipse LV100ND، NIKON CORPORATION، توکیو، ژاپن) مشاهده و تصویربرداری شد.
نتایج کمی از مواد مورد بررسی آماری تجزیه و تحلیل شد. از آنالیز واریانس یک طرفه (ANOVA) استفاده شد. اگر P <0.05، نتایج از نظر آماری معنی دار در نظر گرفته شد.
3. نتایج
به منظور بررسی پیکربندی صحیح سیستم ساخته شده ( شکل 5 ) و تنظیم مقدار هیدروژل تجویز شده (با پارامترهای خاص آن)، آزمایش های شرح داده شده در زیر انجام شد.

شکل 5. تصاویری از چاپگر زیستی سه بعدی ساخته شده با تمام عناصر یکپارچه و آزمایش شده. ( الف ) پمپ پریستالتیک، ( ب ) نگهدارنده نازل با نازل گرم شده و اتصال تسمه تایم، ( C ) محور X چاپگر و بستر چاپ سرد شده را مونتاژ کرد، ( D ) نمای کلی از ساختار چاپگر زیستی سه بعدی، ( E ) نمای سیستم چاپ: محفظه ایزوله پمپ و چاپگر “قفس”، ( F ) ظرف ایزوله پمپ با مخزن همزن و سیستم گرمایش.
3.1. آزمایشات پمپ پریستالتیک
به منظور بررسی عملکرد پمپ پریستالتیک تولید شده طراحی ما، میزان جریان در طول زمان و ضربان فشار در حین کار پمپ مورد آزمایش قرار گرفت. بررسی رفتار پمپ به دلیل افزایش متناسب هیدروژل پمپ شده با افزایش سرعت کار پمپ پریستالتیک، امکان دوز کنترل شده بیواینک را فراهم کرد ( شکل 6 A). در حین کار پمپ، نوسان فشار مشاهده شد. آن تغییرات با تکرارپذیری وقوع در دامنه و فواصل مشخص شد ( شکل 6 B).
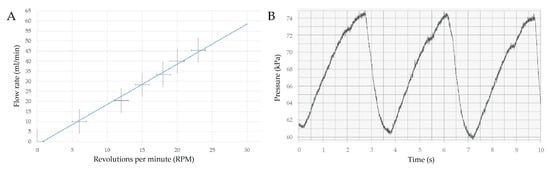
شکل 6. ویژگی پمپ پریستالتیک ساخته شده: ( الف ) سرعت کار (نوارهای خطا میله های انحراف استاندارد (SD) هستند)، ( B ) نوسانات فشار در حین کار.
3.2. تجزیه و تحلیل جریان نازل
منحنی های جریان برای دو هیدروژل مورد بررسی: 5A3G و 6A4G، در شکل 7 ارائه شده است . تغییرات ویسکوزیته به وضوح سیالات غیر نیوتنی را نشان می دهد. علاوه بر محدوده سرعت برش کمتر از 10s -1 ، سیالات افت ویسکوزیته مداوم را نشان می دهند و می توانند به عنوان سیالات شبه پلاستیک (رقیق کننده برشی) طبقه بندی شوند. مدل Ostwald de Waele(μeff= k ·γn – 1)(�eff=ک·�n–1)می توان برای تقریب رابطه بین ویسکوزیته موثر استفاده کردμeff�effو نرخ برشγ�، که در آن k پارامتر قوام ویسکوزیته و n شاخص قانون توان است. مقادیر ضریب k = 5.6 Pa·s، n = 0.76 و k = 2.5 Pa·s، n = 0.70 برای 5A3G و 6A4G به ترتیب برای تقریبی داده ها استفاده شد که در شکل 7 نشان داده شده است .
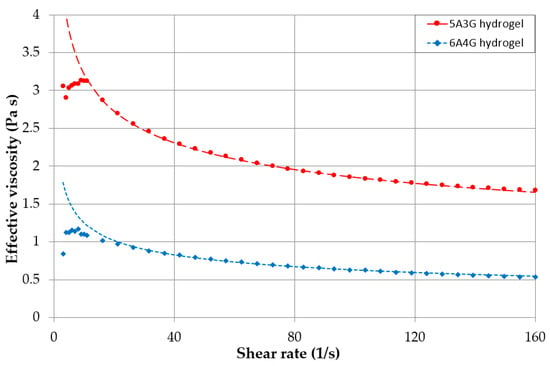
شکل 7. منحنی های جریان (ویسکوزیته موثر در برابر نرخ برش) برای هیدروژل های 5A3G و 6A4G (ترکیبات آلژینات و ژلاتین).
یک رابطه ساده از هاگن-پوازی برای جریان های آرام سیالات نیوتنی را نمی توان در این مورد اعمال کرد. بنابراین، شبیهسازیهای عددی جریان سیال غیرنیوتنی با حلکننده ANSYS CFX طبق تعریف ارائهشده در بخش 2.3 انجام شد .
توزیع سرعت و نرخ کرنش برشی به دست آمده از شبیه سازی ها در ورودی نازل در شکل 8 A,B برای هیدروژل 5A3G ارائه شده است. نتایج برای هیدروژل 6A4G فقط کمی متفاوت بود. آنها به وضوح نشان دادند که طول ورودی در نازل بسیار کوتاه است. جریان به طور کامل توسعه یافت (شکل پروفیل سرعت ثابت شد) در فاصله نیمی از قطر نازل از ورودی آن. این با طول ورودی مطابق با رابطه ( Le = 0.05 · D · Re ) [ 37 ] بود که برای چنین اعداد رینولدز کم مانند موارد مورد تجزیه و تحلیل، بسیار کوتاه است. توزیع سرعت و نرخ کرنش برشی کاملا توسعه یافته در امتداد شعاع نازل در شکل 9 A,B برای هیدروژل های 5A3G و 6A4G و همچنین برای یک سیال نیوتنی (با چگالی یکسان، اما ویسکوزیته ثابت برابر با 0.8 Pa·s) نشان داده شده است. به طور کلی، هیچ تفاوتی در توزیع برای هر دو هیدروژل مشاهده نشد. علاوه بر این، توزیع سرعت برای هیدروژل ها تفاوت معنی داری با تابع سهموی برای مایعات نیوتنی نداشت. با این حال، واضح بود که ویسکوزیته موثر بالاتر برای نرخ های برشی پایین باعث کاهش حداکثر سرعت هیدروژل ها در محور لوله می شود. به طور مشابه، توزیع نرخ کرنش برشی در امتداد شعاع با تابع خطی برای سیال نیوتنی متفاوت است.
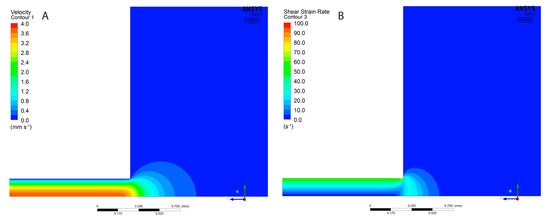
شکل 8. خطوط سرعت ( A ) و نرخ کرنش برشی ( B ) در ورودی نازل برای هیدروژل 5A3G.
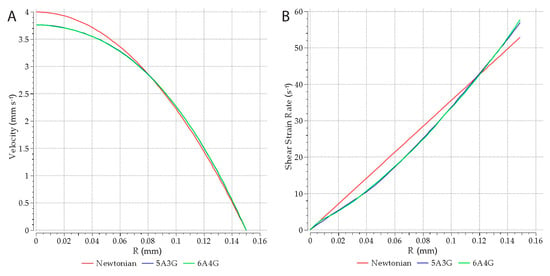
شکل 9. نموداری از توزیع سرعت کامل ( A ) و نرخ کرنش برشی در امتداد شعاع نازل ( B ).
با توجه به کوتاه بودن طول ورودی، فشار هیدروژل ها به صورت خطی در طول نازل کاهش یافت. مقادیر فشار گیج در ورودی نازل (یعنی فشار تولید شده توسط پمپ) به دست آمده از شبیه سازی ها به ترتیب برابر با 26.3 کیلو پاسکال و 9.4 کیلو پاسکال برای هیدروژل های 5A3G و 6A4G بود.
3.3. ارزیابی حامل نازل و بلوک گرمایشی
حامل نازل جدید طراحی و تولید شده و بلوک گرمایشی به منظور بررسی توزیع مناسب بیواینک و دقت چاپها آزمایش شدند. بالاترین سطح دقت برای پرینت های انجام شده در دمای اواسط آزمایش شده 37 درجه سانتی گراد به دست آمد. در دمای 34 درجه سانتیگراد آزمایششده، هیدروژلهای 5A3G و 6A4G بیش از حد متراکم بودند، که مانع اکستروژن آن شد و باعث بدتر شدن کیفیت چاپ شد. در دمای 40 درجه سانتی گراد، این هیدروژل ها به دلیل کاهش ویسکوزیته ناشی از دمای اکستروژن بالاتر، جریان پذیری بسیار بالایی از خود نشان دادند. بعد مسیر اندازه گیری شده مقطع نسبت به ضخامت مورد نظر مسیر بزرگ شد. این منجر به بدتر شدن کیفیت چاپ شد، زیرا یک مسیر ضخیم تک اکسترود شده روی بستر چاپ سرد نمیتوانست شکل خود را حفظ کند. این به دلیل نشت تصادفی مواد از نازل بود.
3.4. ارزیابی تخت چاپ سرد
به لطف بستر چاپی خنک، پرینتها به بیرون ریخته نشدند و شکل خود را با دقت ابعادی بالا حفظ کردند. دمای ایده آل برای انجماد فوری هیدروژل 10 درجه سانتی گراد بود. این امکان اتصال عرضی سریع ژلاتین را حتی تا 14 لایه فراهم کرد. سیستم برای یکنواختی دما در سطح تخت چاپ بررسی شد ( شکل 10 ). یک تصویر حرارتی با دوربین تصویربرداری حرارتی مادون قرمز FLIR T420 گرفته شد.
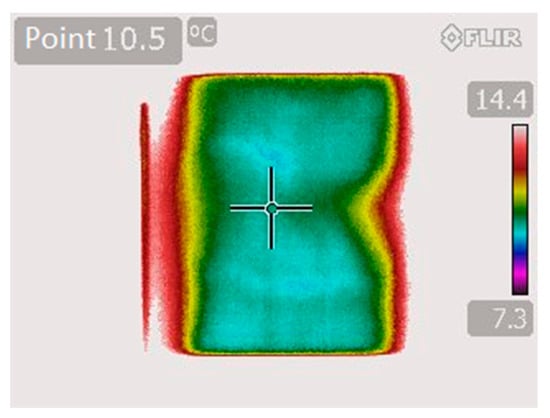
شکل 10. توزیع دما بر روی بستر چاپ بیوپینتر سه بعدی مجهز به سلول پلتیه.
توزیع دما به صورت نقشه رنگی قابل مشاهده است. در نقطه میانی سمت راست تخت چاپی دمای بالاتری مشاهده شد که ناشی از عبور مسیر ترمیستور بین بالای شیشه تخت و سلول پلتیه بود.
3.5. نتایج دقت چاپ
یکی از مهمترین پارامترهای هر چاپگر زیستی سه بعدی دقت چاپ است. این بدان معنی است که ابعاد عنصر چاپ شده دقیقاً مطابق با هندسه CAD از پیش تعریف شده است. ابعاد مدل 13.6 × 13.6 × 11.0 میلی متر (X,Y,Z) با عرض خط 0.28 میلی متر ( شکل 3 B) بود. نتایج بهدستآمده از آزمایش دقت چاپ 11/0 ± 13/62 (mm) برای محور X، 13/63 ± 0/1 (mm) برای محور Y و 10/0 ± 0/5 (mm) برای محور Z ( شکل 11 ) بود. نتایج بهدستآمده تکرارپذیری فرآیند چاپ را نشان میدهد که تحت تأثیر کالیبراسیون مناسب چاپگر و پارامترهای چاپ قرار دارد.
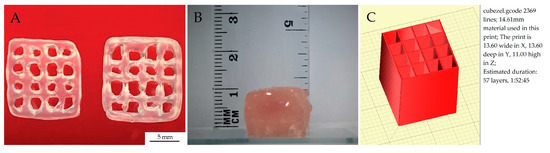
شکل 11. ( الف ) نمای بالای شبکههای چاپ شده بر روی دستگاه اکسترودر مبتنی بر پریستالتیک، مورد استفاده برای آزمایشهای دقت چاپ، ( B ) ارتفاع مدل چاپ شده از 57 لایه، ( C ) مدل چاپ با تعداد لایههای مشخص شده.
3.6. نتایج چسبندگی لایه
مقادیر به دست آمده از تست چسبندگی مقادیر قدرت چسبندگی برای اتصال تک لایه به لایه بود که مهمترین پارامتر مقاومت عناصر پرینت سه بعدی است. نمونه های چاپ شده با استفاده از سیستم ما می توانند فشار 9.06 ± 98.1 (kPa) را تحمل کنند ( شکل 12 ).
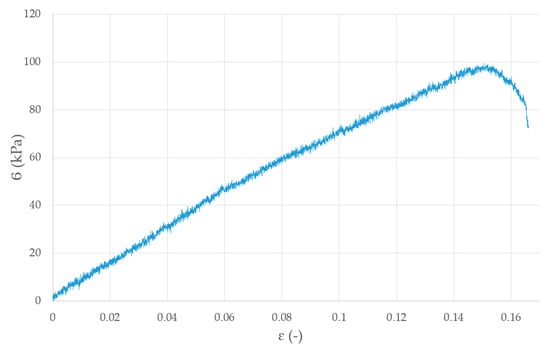
شکل 12. نمودار تنش چسبندگی استاتیک برای نمونه 30 × 10 × 0.35 میلی متر برای هیدروژل 5A3G.
مدل بر روی تغییر لایه تحت نیروی 100 کیلو پاسکال لایه لایه شد. استحکام پیوند لایه به اندازهای بالا است که بتواند نیروهای داخل بدن انسان را تحمل کند، به عنوان مثال، فشارهای وارد شده به حالب در طول جریان ادرار 20-40 میلیلیتر بر ثانیه، تا 100 کیلو پاسکال است [ 38 ].
3.7. نتایج برای ارزیابی زنده ماندن سلول ها پس از چاپ زیستی مستقیم
این مطالعه بیولوژیکی تأثیر ساختار پرینتر سه بعدی (پمپ پریستالتیک، مخزن و لوله های بیوئینک تثبیت شده با درجه حرارت، یک نازل گرم شده) را بر زنده ماندن سلول ارزیابی کرد. نتایج نشان داد که گرم کردن نازل در دمای بالای 37 درجه سانتیگراد (که بهینه برای سلولهای یوکاریوتی در نظر گرفته میشود) روی زندهمانی سلول تأثیری نمیگذارد، اما اگر در بیووینک غوطهور شوند، حتی میتواند بقای آنها را افزایش دهد. شکل 13 نتیجه ارزیابی زنده ماندن سلول را برای چاپ های تولید شده با نازل گرم شده تا دمای 34، 37 و 40 درجه سانتی گراد نشان می دهد. اگرچه این تفاوتها تفاوت معنیداری نداشتند، میتوان متوجه شد که بقای سلول برای نازل با دمایی برابر با 40 درجه سانتیگراد بالاترین میزان بود ( شکل 13 ). این به دلیل ویسکوزیته پایین هیدروژل ها در دمای 40 درجه سانتیگراد بود که کمترین تنش برشی را ایجاد کرد همانطور که قبلا نشان داده شد [ 33 ].
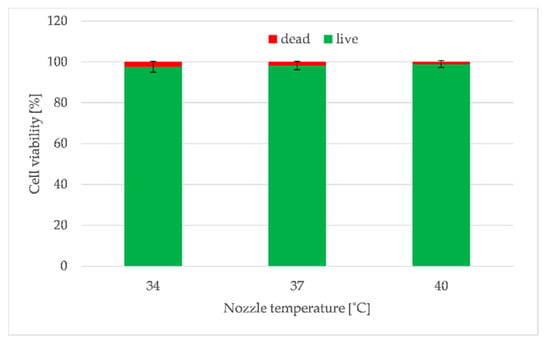
شکل 13. تأثیر دمای مختلف اکستروژن (34، 37 و 40 درجه سانتی گراد) بر روی سلول های اندوتلیال (خط EA.hy 926) زنده ماندن هیدروژل 5A4GM. با اجازه مرجع [ 33 ] تکثیر شده است. حق چاپ MDPI 2019.
نتایج زندهمانی سلولها نیز نشان داد که نه فرآیند آمادهسازی بیوئینک و نه سطوح مختلف فشار (که برای اکسترود کردن هیدروژل در دمای متغیر لازم است) تأثیر منفی بر سلولها نداشتند. علاوه بر این، راه حل های طراحی شده یک چاپگر زیستی توسعه یافته، هم در محدوده مخزن گرم با عملکرد مخلوط کردن، و هم در کل سیستم تامین و اکسترود بیوئینک، شرایطی را فراهم می کند که الزامات تکنیک های افزودنی برای چاپ مستقیم با استفاده از هیدروژل را برآورده کند. حاوی مواد بیولوژیکی به شکل سلول های زنده است.
4. بحث
چاپ سه بعدی فرصتی را برای ایجاد عناصر فردی و شخصی، از جمله مواردی که برای کاربردهای پزشکی استفاده می شود، فراهم می کند. علاوه بر این، به فرد اجازه می دهد تا عناصری از مواد مختلف از جمله ترموپلاستیک ها، هیدروژل ها و فلزات بسازد.
در این کار، هم طراحی اکسترودر فاز مایع و هم پارامترهای چاپ به سمت چاپ زیستی جهت گیری شدند. در این مورد، موضوع کلیدی در انتخاب پارامترهای بهینه چاپ، تعیین ویژگی های اصلی ماده مورد استفاده برای چاپ، مانند ویسکوزیته، تراکم و قابلیت اکسترودپذیری آن است. این پارامترها به نوبه خود مستقیماً به غلظت اجزا و دمای آنها بستگی دارد. در مورد ما از ژلاتین و آلژینات سدیم در غلظت های مختلف برای تهیه هیدروژل استفاده شد. همانطور که خواص مواد را تعیین کردیم، توانستیم محدوده بهینه بهترین پارامترهای کاری اکسترودر فاز مایع تولیدی و قطر نازل را برای رسوب گذاری اجسام با دقت مورد نیاز انتخاب کنیم.
سیستم طراحی شده بار زیادی به هیچ یک از عناصر متحرک چاپگر اضافه نمی کند. وزن اضافی عناصر بر روی قاب چاپگر قرار می گیرد که بر حمل اکسترودر تأثیر نمی گذارد. این سیستم سرعت و شتاب چاپ را به حداکثر می رساند زیرا بیشتر جرم اکسترودر از قاب متحرک حذف می شود. ارتعاشات دستگاه در حین چاپ به لطف این راه حل به حداقل می رسد. حذف جرم اضافی از کالسکه اکسترودر به ما امکان می دهد از لرزش پرینتر سه بعدی سبک وزن نیز جلوگیری کنیم، به خصوص در هنگام شتاب و کاهش سرعت با سرعت بالا. با توجه به این بهبود، ما نقص های چاپی مانند “تغییر لایه” را در چاپ های خود مشاهده نمی کنیم – مصنوعی که بر تمام لایه های بعدی تأثیر می گذارد و به دلیل وزن زیاد توسط موتور پله ای شروع می شود. علاوه بر این، سیستم ما ممکن است با انواع چاپگرهای سه بعدی منبع باز استفاده شود. این برای استفاده با موتورهای پله ای NEMA 17 طراحی شده است که در اکثر سیستم های منبع باز یافت می شود. این امکان را برای نصب با حداقل بازسازی، کدگذاری یا حذف قطعات فراهم می کند. یک اکسترودر ترموپلاستیک پیش فرض را می توان با یک نازل متصل به سیستم از طریق یک لوله جایگزین کرد. علاوه بر این، این سیستم با اندازه سوزن 150 تا 800 میکرومتر سازگار است، در حالی که اکسترودرهای خمیر موجود بیشتر از نازل هایی با قطر حداکثر 4 میلی متر استفاده می کنند [ 9 ، 10 ، 11 ، 12 ]. در ساخت ما، قطر سوزن را می توان با ویسکوزیته مواد مورد استفاده تنظیم کرد و به راحتی قابل تغییر است زیرا ما از اتصال قفل Luer استفاده می کنیم. به دلیل شبیه سازی عددی انجام شده، سیستم می تواند قطر نازل مناسب و فشار مورد نیاز را متناسب با ویسکوزیته مواد و دمای اکستروژن محاسبه کند. بنابراین، در سیستم ما می توانیم پارامترهای چاپ را حتی در سطح آماده سازی هیدروژل تغییر دهیم. علاوه بر این، محاسبات جریان نازل به ما امکان میدهد پیشبینی کنیم که آیا فشار اکستروژن مورد نیاز برای یک هیدروژل مشخص (و دقت مورد انتظار چاپها) برای سلولها کشنده است یا خیر، با فرض اینکه فشار کشنده برای سلولهای زنده بالاتر از 160 کیلو پاسکال باشد [ 39 ]. با تشکر از همه پیشرفتهای ارائه شده در سیستم، پارامترها را میتوان قبل از چاپ تنظیم کرد تا از اشتباهات اولیه آزمایشی جلوگیری شود.
نتایج بررسی پمپ پریستالتیک ساخته شده ( شکل 6 الف) عملکرد صحیح دستگاه را تایید کرد. علاوه بر این، اندازه گیری نوسانات فشار نشان داد که این نوسانات قابل تکرار هستند ( شکل 6 B). آزمایشات نشان داد که این دستگاه به روشی مناسب طراحی و ساخته شده است و الزامات میکرو اکستروژن مواد با ویسکوزیته بالا که به عنوان جوهر در فرآیند چاپ زیستی استفاده می شود را برآورده می کند.
روش اعمال شده برای خنک کردن بستر چاپی مشابه راه حل موجود در چاپگر زیستی BioX6 است که توسط CELLINK (CELLINK ® ، گوتنبرگ، سوئد) تولید شده است، که در حال حاضر یکی از پرفروش ترین چاپگرهای زیستی تجاری در جهان است [ 40 ]. معرفی یک تخت چاپ با دمای قابل کنترل به سیستم ما به دلیل مهار اثر ریختن هیدروژل بدون به خطر انداختن بقای سلول، کیفیت چاپ را بهبود می بخشد. بنابراین، می توان نه تنها از هیدروژل های شیمیایی با پیوند متقابل، بلکه از هیدروژل های متقاطع فیزیکی نیز استفاده کرد که به تغییر دما بستگی دارد. ترکیب طرح های کاربردی به همراه قابلیت تنظیم سیستم با ویسکوزیته بیواینک و دمای کنترل شده بستر چاپ، سیستمی با تکرارپذیری بسیار بالا در ابعاد پرینت ایجاد می کند. این ویژگی علاوه بر این، استفاده از ماشین را در مهندسی بافت بهبود می بخشد. علاوه بر این، آزمون چسبندگی لایه نشان داد که استحکام پیوند بین هر لایه از پرینتها در سطح 100 کیلو پاسکال است. از آنجایی که استحکام کششی عناصر پرینت سه بعدی با اتصال لایه به لایه [ 41 ] تعیین میشود، پیشرفتهای سیستم ما برای دوام چاپ عناصری را ایجاد میکند که میتوانند در بدن انسان پیادهسازی شوند.
همه چاپگرهای زیستی تجاری دارای سرنگ های بسیار کوچک و با حجم محدود هستند [ 31 ، 32 ، 40 ]. سیستم پرینت زیستی سه بعدی ما دارای یک مخزن زیستی است که می تواند در حین کار دوباره پر شود و امکان هم زدن و گرم کردن مخزن زیستی را فراهم می کند، چیزی که تجمع و رسوب سلولی را به حداقل می رساند. بنابراین، توزیع یکنواخت سلولها در بیوئینک برای کل فرآیند چاپ در یک سطح حفظ میشود. از آنجایی که این سیستم دارای یک مخزن قابل شارژ است، به طور بالقوه می تواند پرینت های بسیار بزرگ تری نسبت به سایر چاپگرهای زیستی تجاری تولید کند و در عین حال سطح بالایی از نقشه برداری مدل سه بعدی را حفظ کند.
برخی از سیستمهای چاپ زیستی شامل لامپهای فرابنفش (UV) برای استریل کردن محفظه چاپ زیستی هستند [ 31 ]. سیستمهای دیگر بر پایه عناصر تک استفاده هستند [ 32 ]. سیستم ما می تواند از هر دو روش استریلیزاسیون استفاده کند یا می تواند اتوکلاو شود. این به دلیل این واقعیت است که تمام عناصر در تماس با سلول ها در برابر دما مقاوم هستند، به راحتی می توان آنها را جدا کرد و استریل کرد. این امر نه تنها بر محیط زیست، بلکه بر هزینه چاپ تکی نیز تأثیر مثبت دارد.
فرآیند استریلسازی آسان، سریع و ارزان قطعات سیستم چاپ در تماس با مواد بیولوژیکی همراه با امکان اعمال مخزن بیواینک قابل پر کردن، از مزایای اصلی استفاده از پمپ پریستالتیک در مقایسه با سایر تکنیکهای چاپ زیستی مبتنی بر اکستروژن است.
5. نتیجه گیری ها
تلاش های مشترک در سطح بین المللی به توسعه سریع فناوری چاپ زیستی، هم در طیف مواد مورد استفاده در چاپ و هم در خود چاپگرهای زیستی کمک می کند. چاپ بیولوژیکی مستقیم برای استفاده در مهندسی بافت، به دلیل دقت پرینتها در رابطه با مدل CAD، بقای سلولهایی که مواد بیولوژیکی معلق در هیدروژل را تشکیل میدهند و شرایط استریل در طول کار چاپگر را حفظ میکنند، نیازمند الزامات دقیقی است. در مورد ما، تاکید اصلی بر روی دستگاه بود که امکان چاپ زیستی کارآمد و مستقیم را فراهم می کند. ما سیستمی را طراحی و آزمایش کرده ایم که با نیازهای مهم مطابقت دارد.
دمای قابل کنترل عناصر سیستم یکی از مهمترین مسائل برای اطمینان از ایمنی سلول ها و خواص مناسب یک بیوئینک است. سیستم ما برای ارائه انتخاب دمای اکستروژن در محدوده 30 تا 40 درجه سانتیگراد طراحی شده است. اگرچه دمای 37 درجه سانتی گراد به عنوان دمای بهینه برای سلول های یوکاریوتی در نظر گرفته می شود، اما نتایج نشان داد که گرم کردن نازل بالای این حد می تواند یک ویژگی بسیار ارزشمند اکسترودر باشد. بیواینک که در طول اکستروژن تا دمای 40 درجه سانتیگراد گرم می شود، بر روی زنده ماندن سلول تأثیر نمی گذارد و حتی می تواند بقای آنها را افزایش دهد زیرا دمای بالا ویسکوزیته هیدروژل و تنش برشی را کاهش می دهد و در نتیجه فشار مورد نیاز برای اکستروژن را کاهش می دهد.
برای دستیابی به دقت مناسب در پرینتها، موقعیت نازل و حجم بیواینک اکسترود شده بسیار مهم است. ویژگی های پمپ به تنظیم آن با شرایط اکستروژن کمک می کند. پالایش و تنظیم پارامترهای چاپگر مانند سرعت اکستروژن، ویسکوزیته بیواینک، قطر نازل، دمای هیدروژل و دمای بستر چاپ سرد شده با اکسترود کردن مقدار مواد طراحی شده به شکل تعریف شده روی بستر چاپ، پرینت های مناسبی را فراهم می کند. ادغام بستر چاپی خنکشده Peltier، دامنه موادی را که میتوان در سیستم استفاده کرد، گسترش میدهد، زیرا امکان اتصال متقابل فیزیکی فوری هیدروژلهای قابل درمان حرارتی مانند مخلوطهای حاوی ژلاتین را فراهم میکند.
شبیه سازی عددی جریان هیدروژل در اکسترودر به فرد اجازه می دهد تا به راحتی شرایط جریان را آزمایش کند و طراحی نازل را با ویسکوزیته ماده خاص تنظیم کند. همانطور که کل سیستم در نرم افزار CAD مدل شده است، نازل را می توان به راحتی تغییر داد تا اطمینان حاصل شود که مواد ارائه شده به درستی اکسترود شده است، و فشار داخلی در شیلنگ از 160 کیلو پاسکال تجاوز نمی کند، که حداکثر فشار برای حفظ قابلیت تکثیر سلولی است. .
همه عناصر برای ایجاد چاپگری طراحی شده اند که الزامات چاپ سه بعدی برای مهندسی بافت را برآورده می کند. راه حل های ارائه شده در سیستم ما می توانند به پیشرفت در استفاده بالینی از چاپ زیستی کمک کنند. همچنین میتواند معرفی واقعی فرآیند و تکنیکهای چاپ زیستی در تولید مثل بافتهای انسانی را تسریع بخشد. تمام راه حل های طراحی شده برای سیستم چاپگر زیستی ما می توانند ویژگی های بسیار ارزشمندی برای کاربردهای اضافی علاوه بر داربست های بافتی و کاربردهای پزشکی داشته باشند. استفاده از آنها در هر چاپگر سه بعدی دیگری می تواند فرآیند آزمایش مواد جدید را بسیار ارزان تر و سریع تر کند.